问题
问答题
实验室有一瓶新配制的稀盐酸(HCl气体溶于水得到的混合物为稀盐酸),其标签的部分内容如图所示.
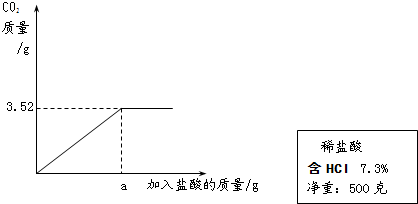
(1)计算该稀盐酸中氯元素的质量分数.
(2)某实验小组用这种稀盐酸测定某石灰石样品中碳酸钙的质量分数,实验过程是:称取10g石灰石样品研成粉末,向其中加入7.3%的稀盐酸,产生二氧化碳的质量与加入盐酸的质量关系如图所示.(假设样品中的杂质都不和盐酸反应)计算石灰石样品中碳酸钙的质量分数.
答案
(1)该稀盐酸中氯元素的质量分数为
×100%=7.1%500g×7.3%× 35.5 36.5 500g
(2)由图象可知该样品完全反应后生成的二氧化碳质量是3.52g;
设石灰石样品中碳酸钙的质量为x
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 44
x 3.52g
=100 x 44 3.52g
x=8g
石灰石样品中碳酸钙的质量分数为:
×100%=80%8g 10g
答:(1)该稀盐酸中氯元素的质量分数为7.1%.(2)石灰石样品中碳酸钙的质量分数是80%;
