根据下列实验现象,所得结论正确的是:( )
| 实 验 | 实验现象 | 结 论 |
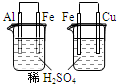
| A |
左烧杯中铁表面有气泡,右边烧杯中铜表面有气泡 | 活动性:Al>Fe>Cu |
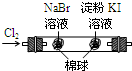
| B |
左边棉花变为橙色,右边棉花变为蓝色 | 氧化性:Cl2>Br2>I2 |
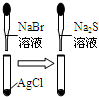
| C |
白色固体先变为淡黄色,后变为黑色 | 溶解性:AgCl>AgBr>Ag2S |
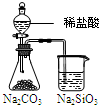
| D |
锥形瓶中有气体产生,烧杯中液体变浑浊 | 非金属性:Cl>C>Si |
A.A
B.B
C.C
D.D
A、左烧杯中铁作正极,表面有气泡生成,铝做负极,右边烧杯中铜作正极,表面有气泡生成,铁做负极,负极金属活泼性>正极金属活泼性,故活动性:Al>Fe>Cu,故A正确;
B、氯气能氧化溴离子和碘离子,置换出溴单质和碘的单质,但是潮湿的氯气具有漂白性,所以棉花变为白色,故B错误;
C、由沉淀的转化原理:化学反应向着生成更难溶物质的方向进行,氯化银为白色,溴化银为淡黄色,硫化银为黑色,溶解性:AgCl>AgBr>Ag2S,故C正确;
D、向碳酸钠中加盐酸,锥形瓶中有气体产生,说明盐酸酸性强于碳酸,烧杯中液体变浑浊,说明碳酸酸性强于硅酸,所以得酸性强弱:盐酸>碳酸>硅酸,而判断元素的非金属性强弱是看元素最高价氧化物对应的水化物的酸的酸性,故D错误.
故选AC.