问题
问答题
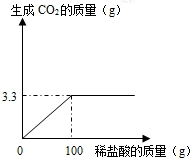
某课外活动小组为测定当地石灰石中含碳酸钙的质量分数,取来了一些矿石,准确称取样品10g放于烧杯中(杂质既不溶于水,也不与稀盐酸反应,也不分解),向其中加入足量的稀盐酸,根据实验测得的数据绘制下图.
问:(1)10g样品可以产生多少克二氧化碳
(2)该样品中碳酸钙的质量分数
(3)一吨该石灰石可制成多少吨生石灰.(已知:CaCO3高温CaO+CO2↑)
答案
(1)由图中曲线可知:曲线不再上升并保持水平时,对应的纵坐标数值为3.3g,这个数值即为产生二氧化碳的质量.
(2)设样品中碳酸钙的质量分数为x.
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 44
10g×x 3.3g
=100 44
,x=75%10g×x 3.3g
(3)设生成生石灰的质量为y.
CaCO3
CaO+CO2↑ 高温 .
100 56
1t×75% y
=100 56
,y=0.42t1t×75% y
答:(1)产生3.3g二氧化碳.
(2)样品中碳酸钙的质量分数为75%.
(3)生成生石灰0.42t.
