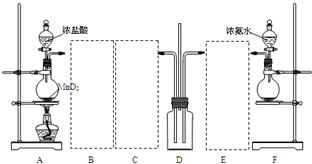
如图,某学习小组利用下列装置探究氯气氨气之间的反应,其中A、F分别为氯气和氨气的发生装置,D为纯净的氯气和氨气的反应装置.
请回答下列问题:
(1)装置F中烧瓶内的固体可选用______
A、氯化铝 B、生石灰 C、五氧化二磷 D、烧碱
(2)实验中所用的浓盐酸的质量分数为36.5%,其密度为1.19 g/cm3,则其物质的量浓度为______(保留两位小数),在标况下需______L(保留两位小数)氯化氢溶于1L水中才可得此浓度的盐酸.
(3)虚线框内应添加必要的除杂装置,请将除杂装置中相应的试剂名称填入下列空格中:B______;C______;E______.
(4)装置D内出现白烟并在容器内壁凝结,鉴定该固体是氯化铵所需要的试剂有:______.
(5)有同学认为D中除了有氯化铵生成外,还应有其他物质生成,你认为他的理由是______.如果D中气体未出现红棕色,也没有白烟产生,则D中发生反应的化学方程式是______.
(1)A、C都能够和氨水反应,无法制取氨气;B、D都可以使浓氨水迅速产生氨气,故答案的:BD;
(2)1L溶液的质量为:1.19×1000×1=1190(g),c(HCl)=
÷1=11.9(mol/L),1L溶液中,n(HCl)=11.9mol,标况下,V(HCl)=22.4×11.9=266.56(L),故答案是:11.9mol/L;266.56;1190×36.5% 36.5
(3)氯气在饱和食盐水中溶解度较小,故用饱和食盐水出去氯气中混有的氯化氢,所以B为饱和食盐水;浓硫酸不与氯气反应,干燥效果好,故制取氯气常用浓硫酸作干燥剂,故C为浓硫酸;E是干燥氨气的试剂,通常使用碱石灰,故E为碱石灰,
故答案为:饱和食盐水;浓硫酸;碱石灰;
(4)鉴定该固体是氯化铵,需要分别鉴定铵离子和氯离子,铵离子检验方法是:先加入溶液,产生使红色石蕊试纸变蓝的气体,证明铵离子存在;氯离子检验方法是:先滴加硝酸银溶液,产生沉淀,再加入稀硝酸,沉淀不溶解,证明氯离子存在,故答案是:NaOH溶液和湿润的红色石蕊试纸;硝酸银溶液和稀硝酸;
(5)若有氯化铵生成,根据电子守恒,氯气中的氯元素得到电子,化合价降低,一定还有失去电子,化合价升高的元素;由于D中气体未出现红棕色,也没有白烟产生,可以断定氨气中的氮元素应后生成了氮气,发生的反应为2NH3+3Cl2═N2+6HCl,
故答案为:化合价如果只生成氯化铵,化合价只有降而没有升,不符合氧化还原反应得失电子相等的规律;2NH3+3Cl2═N2+6HCl.