问题
问答题
氯酸钾与浓盐酸在一定温度下反应会生成绿黄色的易爆物二氧化氯,反应的化学方程式为:
2KClO3+4HCl(浓)═2KCl+2ClO2↑+Cl2↑+2H2O
(1)用双线桥表示上述反应中电子转移的方向和数目______.
(2)浓盐酸在该反应中表现的性质是______(填序号).
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(3)上述反应产生0.2 mol Cl2时,转移的电子数约为______.
答案
(1)KClO3中Cl元素由+5价降低为+4价,HCl中Cl元素由-1价升高为0,反应中转移2e-,则双线桥表示反应中电子转移的方向和数目
为
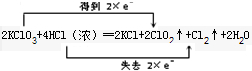
,故答案为:

;
(2)由反应可知,HCl中部分Cl元素的化合价升高,体现还原性,部分化合价不变生成盐表现酸性,故答案为:②;
(3)由反应可知,生成1molCl2时,转移2mol电子,则产生0.2 molCl2时,转移的电子数约为0.4×6.02×1023=2.408×1023,故答案为:2.408×1023.

