问题
问答题
在实验室里,同学们做氧气的制取、性质的分组实验,实验中各小组要消耗两瓶氧气.经计算这两瓶氧气在通常状况下的质量共约为0.72g,若要用10%的过氧化氢溶液和MnO2来制取氧气:
(1)至少需要向每个实验小组提供该溶液多少克?
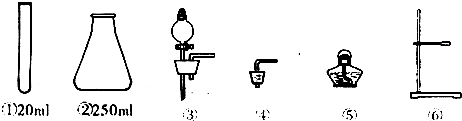
(2)实验准备室中有下列仪器,为保证同学们安全顺利地制取氧气,应选择的仪器有______(写序号)提示:10%过氧化氢溶液的密度为1.04g/cm3.
答案
(1)设生成0.72g氧气时所需的过氧化氢溶液的质量是x
2H2O2
2H2O+O2↑ MnO2 .
68 32
x×10% 0.72g
=68 32 x×10% 0.72g
x=15.3g
答:至少需要向每个实验小组提供该溶液15.3克.
(2)7.65g10%过氧化氢溶液的体积为:
≈14.71cm3=14.71mL15.3g 1.04g/cm3
所以反应的容器应该是②250ml的锥形瓶,20mL的试管做反应容器体积相对14.71mL来说太小,不利于气体制取,选择②后再选择仪器③,这样搭配有利于反应顺利进行且能对反应速度进行控制,因此不选装置④,该过程不需要加热所以不选⑤,也不用铁架台固定,所以不选⑥,只用②③便能顺利实验.
故答案为:(1)至少需要向每个实验小组提供该溶液15.3g
(2)②③
