问题
填空题
某校化学兴趣小组用如图所示过程除去AlCl3中含有的Mg2+、K+杂质离子,并尽可能减少AlCl3的损失.请回答下列问题
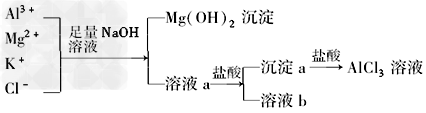
(1)写出混合物中加入足量氢氧化钠溶液时,溶液中发生反应的离子方程式:________、________、________.氢氧化钠溶液能否用氨水代替,为什么?______________________.
(2)溶液a中存在的离子有________;在溶液a中加入盐酸时需控制溶液的pH,为什么?________;为此,改进方法是____________________.
(3)为了研究AlCl3晶体的性质,在得到AlCl3溶液后,如何得到AlCl3晶体?____________________.
答案
(1)Mg2++2OH-===Mg(OH)2↓;Al3++3OH-===Al(OH)3↓;Al(OH)3+OH-===AlO2-+2H2O;不能,因为Al(OH)3不能溶于过量的氨水中,不能将Al(OH)3与Mg(OH)2分开
(2)K+、Cl-、Na+、AlO2-;因为Al(OH)3能溶于强酸,所以需控制pH,防止部分Al(OH)3溶解;在a溶液中通入过量CO2气体
(3)在酸性气氛中对AlCl3溶液进行蒸发结晶
