现用如图1所示的装置制取较多量的饱和氯水并测定饱和氯水的pH.回答有关问题: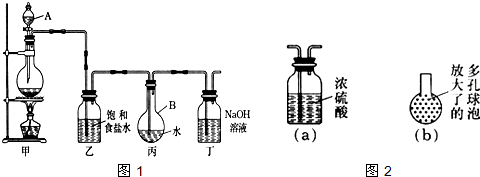
(1)写出有关化学方程式.
装置甲:______;
装置丁:______.
(2)证明氯水已饱和的现象是______.
(3)制取结束时,装置丙的液体中含有最多的微粒是______(水分子除外);装置乙的作用是______.
(4)有如下改进措施或建议,请作出评价:
①在装置乙和丙之间增加如图2(a)所示的装置,你认为有无必要?______.
②在装置丙的长导管下口处,接如图2(b)所示的多孔球泡,这样做的好处是:______.
③若撤去装置乙,直接将装置甲和丙相连.这样做对实验结果的影响是:______.
(1)实验室制取氯气的反应原理:MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O,氯气能和碱反应反应氯化钠、次氯酸钠和水,方程式为:2NaOH+Cl2=NaCl+NaClO+H2O;△ .
故答案为:MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O;2NaOH+Cl2=NaCl+NaClO+H2O;△ .
(2)因饱和溶液中不能溶解氯气以及氯气为黄绿色,所以丙中的导管有气泡溢出水面,且液面上方充满黄绿色气体即可证明氯水已饱和,
故答案为:丙中的导管有气泡溢出水面,且液面上方充满黄绿色气体;
(3)由氯水中成分可知,氯水中含有最多的微粒除了水就是氯气;饱和食盐水来除去氯气中的氯化氢;
故答案为:Cl2;除去氯气中的氯化氢;
(4)①因氯气中含水对制备氯水无影响,所以在装置乙和丙之间不需要增加如图2(a)所示的装置;故答案为:无;
②因多孔球泡的表面积大,能加快氯气溶解的速率,故答案为:增加氯气与水的接触面积,利于氯气溶解;
③因氯气中含有氯化氢,氯化氢溶于水,溶液酸性增强,使测定的pH减小,
故答案为:使测定的pH减小;
