问题
问答题
取一定质量分数的氯化钠溶液117克进行电解,反应的化学方程式为:2NaCl+2H2O
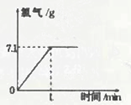
2NaOH+Cl2↑+H2↑,生成氯气的质量与时间的关系如图所示: 电解 .
请计算:
(1)当氯化钠完全反应时,生成氢气多少克?
(2)所取氯化钠溶液的质量分数.
答案
(1)根据图示可知生成氯气质量为7.1g,设要生成7.1g氯气需要参加反应的氯化钠的质量为x,生成氢气质量为y则:
2NaCl+2H2O
2NaOH+Cl2↑+H2↑ 电解 .
117 71 2
x 7.1g y
根据:
=117 71
解得x=11.7g,x 7.1g
根据:
=71 2
解得y=0.2g,所以生成氢气质量为0.2g;7.1g y
(2)所取氯化钠溶液的质量分数:
×100%=10%.11.7 117
故答案为:
(1)0.2g;
(2)10%.
