问题
选择题
某温度下,将Cl2通入KOH溶液里,反应后得到KCl、KClO、KClO3的混合溶液.经测定ClO-与ClO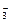 的物质的量浓度之比是1:2,则Cl2与KOH反应时,被还原的氯元素与被氧化的氯元素的物质的量之比是
的物质的量浓度之比是1:2,则Cl2与KOH反应时,被还原的氯元素与被氧化的氯元素的物质的量之比是
A.2:3
B.4:3
C.10:3
D.11:3
答案
D
由已知条件及质量守恒定律写出方程式:
7Cl2+14KOH====11KCl+KClO+2KClO3+7H2O
被氧化的氯为3 mol,被还原的氯为11 mol.即知被还原的氯元素与被氧化的氯元素的物质的量之比为11:3.
