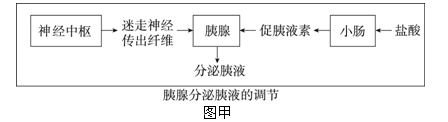
计算题:甲、乙、丙、丁四位同学,用铁与稀硫酸反应,所得有关数据记录如下(误差忽略不计)
| 甲 | 乙 | 丙 | 丁 | |
| 取用稀硫酸质量(克) | 100 | 100 | 100 | 200 |
| 加入金属的质量(克) | x | 1.25x | 2x | 2x |
| 生成H2的质量(克) | 0.4 | 0.5 | 0.6 | 0.8 |
(1)甲同学加入金属铁的质量χ;______
(2)稀硫酸溶液中,H2SO4的质量分数.______.
(1)设甲同学加入铁的质量为x.
Fe+H2SO4=FeSO4+H2↑
56 2
x 0.4g
=56 2
,x 0.4g
x=11.2g;
(2)设稀硫酸溶液中溶质的质量为y.
Fe+H2SO4=FeSO4+H2↑
98 2
y 0.6g
=98 y 2 0.6g
y=29.4g
稀硫酸溶液中,H2SO4的质量分数
×100%=29.4%29.4g 100g
答:甲同学加入金属铁的质量为11.2g;稀硫酸溶液中,H2SO4的质量分数29.4%.
故答案为:
(1)11.2g;
(2)29.4%.