有A、B、C、D、E五种化合物,A为白色固体,B为无色无味的气体,E为不溶于稀硝酸的白色沉淀,它们的关系如图:
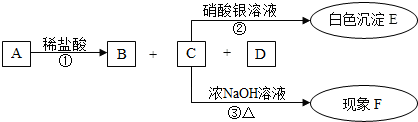
请填空:
(1)白色沉淀E为______.
(2)若现象F为“无明显变化”,则A的化学式可能为______(填字母).
a、Na2CO3;b、MgCO3;c、KHCO3
(3)若现象F为“无色有刺激性气味的气体”,则A可能为______(填化学式),反应③的化学方程式为______.
(1)由图可知,反应①中有稀盐酸,则C是一种盐酸盐,可与硝酸银发生反应生成AgCl白色沉淀,故白色沉淀E为AgCl;(1分)
(2)①若A的化学式为a,则反应方程式为Na2CO3+2HCl=2NaCl+H2O+CO2↑,C为NaCl;
②若A的化学式为b,则反应方程式为MgCO3+2HCl=MgCl2+H2O+CO2↑,C为MgCl2;
③若A的化学式为c,则反应方程式为KHCO3+HCl=KCl+H2O+CO2↑,C为KCl;
若现象F为“无明显变化”,而MgCl2与NaOH反应后生成的Mg(OH)2不溶于水,故排除B;
因此答案为a、c(各1分);
(3)①由题意可知,B为无色无味的气体,故A一定是含有碳酸根离子或碳酸氢根离子的化合物,又由图和题意可知,C与NaOH反应生成无色有刺激性气味的气体,所以,生成气体可能为NH3,故A的化学式为NH4HCO3(1分);
②由上述分析可得A
B+C+D的反应方程式应该是NH4HCO3+HCl=NH4Cl+H2O+CO2↑,故反应③的化学方程式为NH4Cl+NaOH稀盐酸
NaCl+H2O+NH3↑(2分). △ .
