问题
问答题
为了确定某不纯的硝酸钠溶液中所含杂质的成分.一同学设计了如图实验: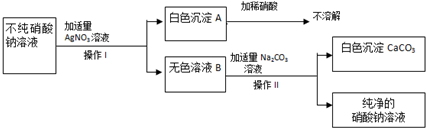
请回答下列问题:
(1)白色沉淀A的化学式为______,I、Ⅱ为______操作.
(2)无色溶液B中加Na2CO3溶液,反应的化学方程式为______.
(3)经分析,原溶液中的杂质由一种或几种物质组成.杂质的成分可能是(填写三种即可)①______②______③______.
答案
(1)Ⅰ步骤中反应是杂质氯化钙和硝酸银反应生成了氯化银沉淀和硝酸钙,化学方程式为:CaCl2+2AgNO3=2AgCl↓+Ca(NO3)2;
由于操作Ⅰ、Ⅱ后得到的是白色沉淀和溶液两部分,所以操作Ⅰ、Ⅱ应该是把液体和不溶于液体的固体分离开了,所以操作Ⅰ、Ⅱ是过滤;
(2)硝酸钙和碳酸钠反应生成碳酸钙沉淀和硝酸钠,反应的化学方程式为:Na2CO3+Ca(NO3)2═CaCO3↓+2NaNO3.
(3)由Ⅱ操作可知无色溶液B是Ca(NO3)2,而Ca2+是来自原溶液中的杂质;由Ⅰ操作可知不溶于稀硝酸的白色沉淀A为氯化银,而Cl-是来自原溶液中的杂质,即原硝酸钠中含有的杂质离子有Cl-和Ca2+,所以杂质的化学式可能为:Ca(NO3)2或NaCl或CaCl2.
故答案为:(1)AgCl,过滤
(2)Ca(NO3)2+Na2CO3=CaCO3↓+2NaNO3
(3)①CaCl2②CaCl2、Ca(NO3)2③CaCl2、NaCl
④CaCl2、NaCl、Ca(NO3)2
