问题
填空题
已知铜在常温下能被稀HNO3溶解,反应为:3Cu+8HNO3═3Cu(NO3)2+2NO↑十4H2O.
(1)请将上述反应改写成离子方程式______.
(2)上述反应中,氧化剂是______.
(3)用单线桥标出上述方程式中电子转移的方向和数目.______.
答案
(1)反应3Cu+8HNO3═3Cu(NO3)2+2NO↑十4H2O中,Cu、NO、H2O在改写成离子反应时保留化学式,则离子反应为3Cu+8H+十2NO3--═3Cu2++2NO↑十4H2O,
故答案为:3Cu+8H+十2NO3--═3Cu2++2NO↑十4H2O;
(2)反应物HNO3中N元素的化合价由+5价降低为+2价,则HNO3为氧化剂,故答案为:HNO3;
(3)Cu元素失去电子,N元素得到电子,转移的电子总数为3×2e-=6e-,单线桥标电子转移的方向和数目为
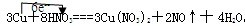
,
故答案为:
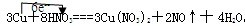
.
