根据下面物质间的转化关系,回答:
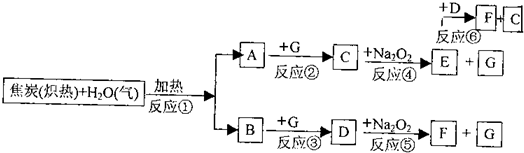
(1)写出B、F物质的化学式B______ F______.
(2)如果1molNa2O2与足量的C物质反应,反应过程中转移的电子数为______个.
(3)反应①②③④中是吸热反应的是(填序号,下同)______,反应①②③④⑤⑥中不是氧化还原反应的是______.
(4)写出反应④⑤的化学方程式:
④______;⑤______;
(5)写出反应⑥在溶液中发生反应的离子方程式(D是足量的)
⑥______
(6)请设计一个课堂小实验,证明反应④是放热反应.______.
焦炭和水蒸气在高温条件下反应生成CO和H2,二者与G反应后的产物都能与Na2O2反应,则G为O2,A、B为CO和H2中的物质,C、D为CO2和H2O中的物质,E、F为Na2CO3和NaOH中的物质,本题的关键是E+D→F+G,由此看判断应是NaOH和CO2的反应,所以A为H2,B为CO,C为H2O,D为CO2,E为NaOH,F为Na2CO3,G为O2,则
(1)由以上分析可知B为CO,F为Na2CO3,故答案为:CO;Na2CO3;
(2)由反应2Na2O2+2H2O=4NaOH+O2 可知,中O以上化合价由-1价升高到0价,1molNa2O2转移1mol电子,应为NA个,
故答案为:NA;
(3)焦炭和水蒸气在高温条件下反应为吸热反应,物质的燃烧、过氧化钠与水或二氧化碳的反应以及酸性氧化物与碱的反应都是放热反应;反应⑥为二氧化碳与NaOH的反应,化合价没有变化,为非氧化还原反应,
故答案为:①;⑥;
(4)反应④为过氧化钠与水的反应,反应的化学方程式为2Na2O2+2H2O=4NaOH+O2,反应⑤为过氧化钠与二氧化碳的反应,反应的化学方程式为2Na2O2+2CO2=2Na2CO3+O2,
故答案为:2Na2O2+2H2O=4NaOH+O2;2Na2O2+2CO2=2Na2CO3+O2;
(5)反应⑥为二氧化碳与NaOH的反应,反应的离子方程式为2OH-+CO2=CO32-+H2O,故答案为:2OH-+CO2=CO32-+H2O;
(6)反应④为过氧化钠与水的反应,反应放热,可用温度计测量温度的变化,具体操作为在烧杯放入少许的水,用温度计记下温度,取少量过氧化钠固体溶于烧杯中,玻璃棒搅拌溶解,用温度计记下温度,温度升高,证明过氧化钠溶于水放热,
故答案为:在烧杯放入少许的水,用温度计记下温度,取少量过氧化钠固体溶于烧杯中,玻璃棒搅拌溶解,用温度计记下温度,温度升高,证明过氧化钠溶于水放热.
