问题
实验题
(16分)某科研小组用MnO2和浓盐酸制备Cl2时,利用刚吸收过少量SO2的NaOH溶液对其尾 气进行吸收处理。
气进行吸收处理。
(1)请写出MnO2和浓盐酸制备Cl2的离子方程式________________.
(2)反应Cl2+Na2SO3+2 NaOH===2NaCl+Na2SO 4+H2O中的还原剂为_______________
4+H2O中的还原剂为_______________ _.
_.
(3)吸收尾气一段时间后,吸收液(强碱性)中肯定存在Cl 、OH
、OH 和SO
和SO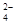 .请设计实验,探究该吸收液中可能存在的其他阴离子(不考虑空气的CO2的影响).
.请设计实验,探究该吸收液中可能存在的其他阴离子(不考虑空气的CO2的影响).
① 提出合理假设.
假设1:只存在SO32-;假设2:既不存在SO3 2-也不存在ClO
2-也不存在ClO ;
;
假设3:_____________.假设4:
② 设计实验方案,进行实验。请在答题卡上写出实验步骤以及预期现象和结论。限选实验试剂:3moL L-1H2SO4、1moL
L-1H2SO4、1moL L-1NaOH、0.01mol
L-1NaOH、0.01mol L-1KMnO4、淀粉-KI溶液、紫色石蕊试液.
L-1KMnO4、淀粉-KI溶液、紫色石蕊试液.
| 实验步骤 | 预期现象和结论 |
步骤1:取少量吸收液于试管中,滴加3 moL L-1 H2SO4至溶液呈酸性,然后将所得溶液分置于A、B试管中. L-1 H2SO4至溶液呈酸性,然后将所得溶液分置于A、B试管中. | |
| 步骤2: | |
| 步骤3: |
答案
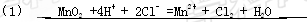
Na2SO3__ .
(3)假设3:__只有ClO___.假设4:SO32-、ClO-都存在
| 实验步骤 | 预期现象和结论 |
步骤1:取少量吸收液于试管中,滴加3 moL L-1 H2SO4至溶液呈酸 L-1 H2SO4至溶液呈酸 性,然后将所得溶液分置于A、B试管中. 性,然后将所得溶液分置于A、B试管中. |  |
| 步骤2:在A试管中滴加紫色石蕊试液 | 若先变红后退 色,证明有ClO-,否则无 色,证明有ClO-,否则无 |
步骤3:在B试管中滴加0.01mol L-1KMnO4溶液 L-1KMnO4溶液 | 若紫红色退去,证明有SO32-,否则无 |