问题
问答题
将碳酸钠晶体(Na2CO3•10H2O)和氯化钠的固体混合物30g,放入一定量的质量分数为10%的盐酸中,恰好完全反应,生成4.4g气体.
求:(1)原混合物中碳酸钠晶体的质量;
(2)反应后溶液中溶质的质量分数.
答案
设原混合物中Na2CO3的质量为x,参加反应盐酸中氯化氢的质量为y,生成氯化钠的质量为z.
Na2CO3+2HCl═2NaCl+H2O+CO2↑
106 73 117 44
x y z 4.4g
=106 x
x=10.6g44 4.4g
=73 y
y=7.3g44 4.4g
=117 z
z=11.7g44 4.4g
(1)原混合物中碳酸钠晶体的质量=10.6g÷
×100%=28.6g106 286
(2)质量分数为10%的盐酸的质量=7.3g÷10%=73g
反应后溶液中溶质的质量分数=
×100%=13.3%30g-28.6g+11.7g 30g+73g-4.4g
答:(1)碳酸钠晶体的质量为10.6g;(2)反应后溶液中溶质的质量分数为13.3%.

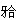 ,磨牙中性关系,上下牙弓Ⅱ度拥挤,口腔卫生差,牙石++,低角,深覆
,磨牙中性关系,上下牙弓Ⅱ度拥挤,口腔卫生差,牙石++,低角,深覆