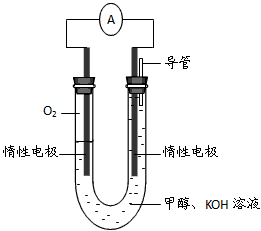
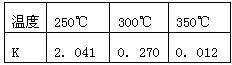以下是小群和小琳同学对一道化学计算题分析、解答、探究的实录.请你一起参与研究并解决相关问题.(计算结果精确到0.1)
[题目]已知:2KClO3═2KCl+3O2↑,将20g氯酸钾和8g二氧化锰混合后放入试管中加热了一段时间,便停止加热,待试管冷却后,称得试管内剩余固体的质量为18.4g.求生成氯化钾的质量.
(1)小群先 根据根据守恒定律求氧气质量,他的计算式是______,然后 根据化学方程式求出了KCl 的质量是______g.
(2)小琳仔细分析了小群上述计算的结果,发现题目数据有问题.请你通过简单的计算,论证她的发现.
(3)小群想了一下,把题目中“20g氯酸钾”改为“a g氯酸钾”,其它数据不变.请你帮小琳算出 a的取值范围是:______≥a>______.
(1)①生成氧气的质量为反应前后试管内固体质量之差:20g+8g-18.4g=9.6g;
②设生成氯化钾的质量为x,
2KClO3
2KCl+3O2↑MnO2 . △
149 96
X 9.6g
∴
=149 x 96 9.6g
解得:X=14.9g;
故答案为:20g+8g-18.4g;14.9克;
(2)所剩固体的质量=14.9g+8g=22.9g>18.4g,所以题目有错误.
(或氯酸钾质量=14.9g+9.6g=24.5g>20g所以题目有错误.)
(3)①如果完全反应后剩余固体质量为18.4g,则生成氯化钾的质量为18.4g-8g=10.4g
设氯酸钾质量为y,
2KClO3
2KCl+3O2↑MnO2 . △
245 149
y 10.4g
∴
=245 x
,149 10.4g
解之得:y=17.1g;
②如果氯酸钾没有反应,则其质量为:18.4-8g=10.4g.
故a的取值范围是:10.4g<a≤17.1g.
故答案为:10.4g<a≤17.1g.

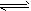 CH3OH(g) ΔH1
CH3OH(g) ΔH1 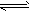 CH3OH(g) + H2O(g) ΔH2
CH3OH(g) + H2O(g) ΔH2