(9分)漂白粉是日常生活中的一种常用消毒剂、杀菌剂和漂白剂。请根据要求回答问题:
(1)漂白粉的有效成分是次氯酸钙[Ca(ClO)2],将氯气通入熟石灰(含水的质量分数略小于1%)即可制取,该反应的化学方程式为 ______________________________。
(2)漂白粉具有漂白作用是因为Ca(ClO)2水解生成了次氯酸(HClO),写出该水解反应的离子方程式_______________________________。
(3)Ca(ClO)2溶液中各离子浓度由大到小的顺序是____________________________。
(4)空气中的二氧化碳可以可增强漂白粉的漂白效果,用化学方程式表示其原理__________________________________________。
(5)漂白粉与洁厕剂等强酸性物质混合使用可生成一种有毒气体,写出该反应的离子方程式________________________________________。
(1)2Cl2+2Ca(OH)2 = CaCl2 +Ca(ClO)2 +2H2O (2分)
(2)ClO-+ H2O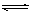 HClO +OH- (2分) (3)c(ClO-)>c(Ca2+)>c(OH-)>c(H+)(1分)
HClO +OH- (2分) (3)c(ClO-)>c(Ca2+)>c(OH-)>c(H+)(1分)
(4)Ca(ClO)2+CO2 + H2O = CaCO3↓+2HClO (2分)(5)ClO- + Cl- + H+ = Cl2↑+ H2O (2分)
(1)考查漂白粉的制取,方程式为2Cl2+2Ca(OH)2 = CaCl2 +Ca(ClO)2 +2H2O 。
(2)次氯酸钙是强碱弱酸盐水解生成次氯酸,方程式为ClO-+ H2O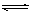 HClO +OH- 。
HClO +OH- 。
(3)次氯酸钙由于水解显碱性,所以溶液中各离子浓度由大到小的顺序是c(ClO-)>c(Ca2+)>c(OH-)>c(H+)。
(4)碳酸的酸性强于次氯酸的,所以碳酸能制取次氯酸,方程式为Ca(ClO)2+CO2 + H2O = CaCO3↓+2HClO 。
(5)在酸性溶液中,ClO-能氧化Cl-生成氯气,方程式为ClO- + Cl- + H+ = Cl2↑+ H2O。
