问题
问答题
取碳酸钠和氯化钠的固体13.6g与质量为73g的稀盐酸恰好完全反应,产生4.4g二氧化碳.计算:
(1)固体混合物中氯化钠的质量;
(2)该稀盐酸中氯化氢的质量分数.
答案
设混合物中碳酸钠质量为X,消耗的稀盐酸中氯化氢的质量为Y,则有
Na2CO3+2HCl=2NaCl+CO2↑+H2O
106 73 44
X Y 4.4 g
=106 X 44 4.4g
X=10.6 g
=73 Y 44 4.4g
Y=7.3 g
固体混合物中氯化钠的质量为13.6g-10.6 g=3g
该稀盐酸中氯化氢的质量分数=
×100%=10%7.3g 73g
答:(1)固体混合物中氯化钠的质量3g;
(2)该稀盐酸中氯化氢的质量分数10%.

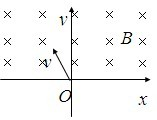
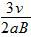 ,正电荷
,正电荷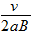 ,正电荷
,正电荷 ,负电荷
,负电荷 ,负电荷
,负电荷