某课外活动小组欲制取次氯酸钠和氯化钠的混合溶液,为提高次氯酸钠含量,用如图所示装置.图中瓶乙盛饱和食盐水,瓶丙盛浓硫酸,分液漏斗A中盛浓盐酸.(据资料显示:Cl2与NaOH在不同温度下,产物不同.在较高温度下易生成NaClO3).
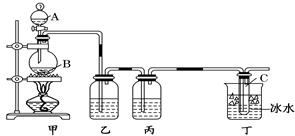
试回答:
(1)烧瓶B中盛 ,试管C中盛 .
(2)有同学认为可以省去某些装置,你认为怎样:
能否省去乙装置? (填“能”或“不能”),理由是
(3)有同学认为还必须加入某些装置,你认为怎样? (填“需要”或“不需要”),如果你认为需要,请指出该装置的作用
(4)丁装置中冰水的作用是 .
(1)MnO2(1分) NaOH溶液 (1分)
(2)不能 (1分)HCl气体进入C中,消耗NaOH,降低NaClO的含量(2分)
(3)需要 (1分)应加上尾气处理装置,防止Cl2污染空气(2分)
(4)防止Cl2与NaOH溶液在温度较高时,发生其他反应(2分)
题目分析:(1)制取Cl2需要浓盐酸与MnO2反应,试管C中盛NaOH溶液。
(2)乙装置能除去Cl2的HCl,如果去掉的话,HCl会与C中的NaOH溶液,降低NaClO的含量。
(3)Cl2有毒,会污染空气,所以应加尾气处理装置,防止Cl2污染空气。
(4)题干中所给信息:“Cl2与NaOH在不同温度下,产物不同.在较高温度下易生成NaClO3”,所以冰水降低温度,防止生成NaClO3。
