黄铁矿的主要成分是FeS2。测定黄铁矿中FeS2含量的两种方法如下图所示:
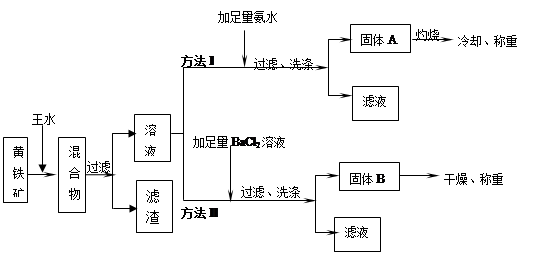
已知:王水(王水是浓盐酸和浓硝酸按体积比为3:1混合而成)与FeS2反应的化学方程式:
FeS2+5HNO3+3HCl=FeCl3+2H2SO4+5NO↑+2H2O
请回答下列问题:
(1)过滤用的玻璃仪器除烧杯、玻璃棒、还有 。
(2)方法II中加足量BaCl2溶液的作用是 ,写出与氯化钡反应的化学方程式 。
(3)通常黄铁矿中会含有其它金属杂质,用方法I测定黄铁矿试样中FeS2的含量时,测定结果会 。(填“偏高”或“偏低”或“不变”) (测定过程中由操作产生的误差可忽略。)
(4)工业上一般不直接用黄铁矿冶炼铁的原因是: 。
(1)漏斗 (2)完全除去硫酸 方程式:BaCl2+H2SO4=BaSO4↓+2HCl
(3)偏高 (4)冶炼过程中有害气体产生(答案合理即可)
题目分析:(1)过滤常使用的玻璃仪器为烧杯、玻璃棒和漏斗;(2)加足量BaCl2溶液主要是完全和溶液中的硫酸完全反应,生成硫酸钡,测定硫酸钡的质量可以根据题目中给出的化学方程式求出FeS2的质量;(3)加足量氨水是为了将其中的铁离子沉淀出来,含有金属杂质会增大沉淀的质量,会使测定结果偏高;(4)黄铁矿中含有大量硫元素,炼制过程中会产生二氧化硫等气体,造成环境污染。
点评:这道题目是对炼铁原理的灵活考查,教科书中给出的是三氧化二铁的炼制,原理基本相同,注意仔细审题,没有学过的知识点题目中均已给出。
