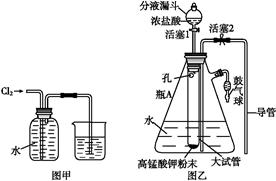
氯水是实验室常需临时配制的一种试剂,图甲所示的是实验室配制氯水时的一种常用装置,图乙是某化学实验小组自行设计的一种配制氯水的装置(图中的鼓气球是一种具有气体单向阀的、可用于向瓶中鼓入空气的仪器)。
(1)氯水需临时配制的原因是: (用化学方程式表示)。
(2)图甲所示装置中,烧杯内的液体是 。
(3)图乙所示装置中,瓶A 内的大试管上端管壁钻有一个小孔,瓶A的名称叫 ,该仪器通常用于
实验中(填基本实验操作的名称)。
(4)用图乙所示装置配制氯水时,操作步骤如下:
①关闭活塞2,打开分液漏斗上口的玻璃塞,再打开活塞1,将少量浓盐酸注入大试管内。
②关闭活塞1,盖上分液漏斗上口玻璃塞。浓盐酸和大试管内的高锰酸钾粉末反应产生氯气。
③轻轻摇动瓶A,使氯气不断溶入水中。
用图乙装置能在较短时间内得到饱和氯水。除了在摇动过程中增大了气体和水的接触面以外,另一个重要原因是 。
分液漏斗中的盐酸应分数次加入试管内。若一次加入太多的盐酸,可能引起的后果是 。
(5)配制氯水完成后,不必拆卸装置即可从瓶A中取用少量氯水,方法是 。
(1)2HClO 2HCl+O2↑
2HCl+O2↑
(2)NaOH溶液 (3)吸滤瓶 减压过滤
(4)氯气在瓶内产生较大压强,增大了氯气的溶解度 瓶内产生过多的氯气,瓶内压强过大会使瓶A的橡皮塞弹开
(5)打开活塞2,关闭活塞1,用鼓气球向瓶A中鼓入空气
(1)氯水中的次氯酸在光照、受热条件下会分解,所以氯水需临时配制。
(2)烧杯内应该盛装能够吸收氯气的NaOH溶液。
(3)注意到图乙装置中瓶A上有一个侧管,是吸滤瓶,是减压过滤的必需仪器。
(4)在大试管中注入浓盐酸后,生成的氯气通过试管上的小孔进入吸滤瓶内与水反应,此时吸滤瓶组成一个密闭装置,压强增大利于氯气的溶解。如果加入盐酸过多,反应过于剧烈,吸滤瓶内压强过大,就可能冲开瓶口的橡胶塞。
(5)取用氯水时可以打开活塞2,通过鼓气球向瓶内鼓入空气,瓶内气体压强增大,氯水就会通过导管流出。
