氯化钠是重要的调味品,是舌尖上最不可缺少的味道。下面三幅示意图分别表示不同的化学反应,但生成物中都有氯化钠。
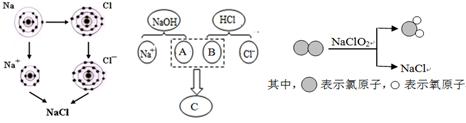
图1 图2 图3
(1)图1是金属钠与氯气反应生成氯化钠的微观示意图。由图1可知,元素的化学性质主要与原子的 (填字母序号)有密切的关系。
A. 最外层电子数 B. 内层电子数 C. 电子层数 D.相对原子质量
(2)图2描述了NaOH溶液与盐酸反应的微观实质,该反应的基本反应类型为 反应,图中A、B、C三种微粒的符号分别是 、 、 。向反应后的液体中滴加酚酞溶液,溶液呈无色。为探究反应后溶液中是否有盐酸剩余,所选试剂不正确的是 。(填字母序号)
A.硝酸银溶液 B.锌粒 C.碳酸钠溶液 D.石蕊
(3)图3所示的四种物质中属于氧化物的是 (填化学式),该反应的化学方程式为 。
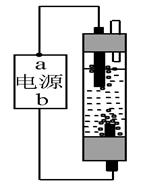
(4)右图是一种家用环保型消毒液发生器,其中发生的主要反应是氯化钠和水在通电条件下反应生成氢氧化钠、氢气和氯气,从能量变化角度看,该反应中将 能转化为化学能。该反应的化学方程式为:
2NaC l + 2H2O  Cl2↑ + H2 ↑ + 2NaOH
Cl2↑ + H2 ↑ + 2NaOH
若电解含氯化钠23.4 g的饱和食盐水,则可制得氢氧化钠的质量是多少?
(1) A
(2) 复分解, OH-、H+、H2O A
(3) ClO2 2NaClO2 + Cl2 ="2" ClO2 + 2NaCl
(4) 电 16g
题目分析:(1)元素的化学性质主要与原子的最外层电子数决定;(2)NaOH溶液与盐酸反应属于复分解反应,有复分解反应的定义图中A、B、C三种微粒的符号分别是OH-、H+、H2O,硝酸银和盐酸不反应,没有现象,无法鉴别;(3)根据氧化物的定义,氧化物由两种元素组成,其中一种是氧气,所以图3所示的四种物质中属于氧化物的是ClO2,化学方程式为2NaClO2 + Cl2 ="2" ClO2 + 2NaCl;(4)从能量变化角度看,该反应中将电能转化成化学能;设可制得氢氧化钠的质量是 g,由题可知
g,由题可知
2NaCl + 2H2O  Cl2↑ + H2 ↑ + 2NaOH
Cl2↑ + H2 ↑ + 2NaOH

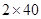


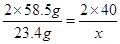 ,解得
,解得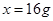
所以若电解含氯化钠23.4 g的饱和食盐水,则可制得氢氧化钠的质量是16g。
点评:常见化学反应及其现象属于必考题型,但是考察形式比较多样,选择题中出现近年也比较多见,注意总结,记忆时注意细心。
