现有四只烧杯,分别盛有稀盐酸、饱和石灰水、碳酸钠溶液中的一种,并向其中滴加了酚酞或石蕊溶液(如下图所示)。
已知:碳酸钠溶液呈碱性,氯化钙溶液呈中性。
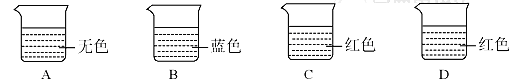
选用下列药品继续实验:铁、氧化钙、氧化铁、稀盐酸、饱和石灰水、碳酸钠溶液请依据实验回答问题:
(1)B 中溶液是 。
(2)取A 中溶液于试管中,加入甲,溶液由无色变为黄色,则甲是 ,反应的化学方程式为 。
(3)取C中溶液于试管中,加入乙,溶液变浑浊;再加入丙,又变澄清,且由红色变为无色,无气泡产生,则乙的化学式为 。
(4)取D中溶液于试管中,加入丁,溶液变浑浊;再加入丙,又变澄清,且由红色变为无色,同时产生气泡。
①用化学方程式表示溶液变浑浊的原因: 。
②最终所得溶液中溶质的组成为 (写出所有可能)。
(1)饱和石灰水或碳酸钠溶液
(2)氧化铁 Fe2O3+6HCl=2FeCl3+3H2O
(3)氧化钙
(4)①Ca(OH)2+Na2CO3==CaCO3↓+2NaOH
②HCl、CaCl2、 NaCl、酚酞或CaCl2、 NaCl、酚酞
(1)石蕊溶液遇酸变红遇碱变蓝,酚酞溶液遇酸不变色遇碱变红色
(2)初中化学中只有Fe3+的溶液显黄色,既然溶液由无色变为黄色,说明有Fe3+
(3)有题目知,最后向浑浊溶液加入丙,没有气体产生,说明浑浊不是碳酸钙形成的,故只能是饱和的石灰水中加氧化钙形成的
(4)由于向浑浊液中加入丙,又变澄清,且由红色变为无色,同时产生气泡,说明浑浊是由CaCO3引起的。由此得出原溶液为Na2CO3溶液,加入丁为Ca(OH)2,浑浊为CaCO3,反应方程式依次为:Ca(OH)2+Na2CO3=CaCO3↓+2NaOH HCl+NaOH=NaCl+H2O CaCO3+2HCl=CaCl2+H2O+CO2↑
