“用微观的眼光看世界”是我们学习化学的重要思想方法。回答下列问题:
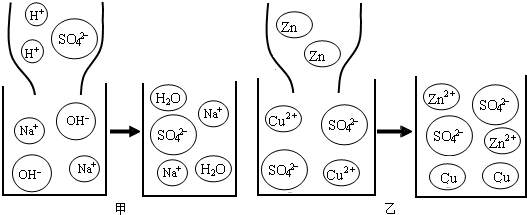
(1)稀硫酸和氢氧化钠溶液发生反应的微观过程如图甲所示。从微观角度分析该反应的实质 ________________________________________;
(2)图乙所示属基本反应类型中的________ 反应;
(3)图甲中为了准确控制反应的进度,可先向氢氧化钠溶液中加入几滴无色酚酞溶液,当二者恰好完全反应时,溶液的颜色变化是________ ,此时溶液中存在的粒子是_______________;
(4)40克固态的氢氧化钠配制成溶液后,能与245克稀硫酸恰好完全反应,则稀硫酸的溶质质量分数是______________ 。
(1)H+ +OH - =H2O(或酸中的H+和碱中的OH-反应生成H2O)
(2)置换
(3)红色液体刚好变成无色液体 Na+ SO42 - H2O
(4)20%
题目分析:从甲图提供的信息可以看出,在反应前后,SO42-和Na+的数目没有发生变化,稀硫酸溶液中的H+和氢氧化钠溶液中的OH –反应生成了H2O;从图乙提供的信息可知,Zn与CuSO4反应,生成了Cu和ZnSO4,故该反应的基本类型是置换反应;当氢氧化钠与稀硫酸恰好完成反应时,溶液中只有硫酸钠和水,溶液呈中性,酚酞溶液由红色刚好变成无色,此时溶液中存在的粒子有硫酸钠解离出来的Na+和SO42 –及构成水的 H2O;设245克稀硫酸中溶质的质量为x。
2NaOH+H2SO4=Na2SO4+2H2O
80 98
40g x
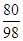 =
=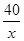
x=49g
稀硫酸的溶质质量分数=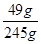 ×100%=20%。
×100%=20%。
