工业上以铝土矿(主要成分是A12O3,含杂质Fe2O3和SiO2)为原料生产铝,其生产流程如下:
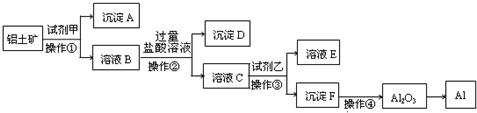
请回答:
(1)工业上Al2O3 冶炼Al所采用的方法是______,化学方程式______
(2)加入试剂甲后发生反应的离子方程式有两个,一是______,二是______.
(3)在溶液B中加入过量盐酸溶液的目的是______.
(4)加入试剂乙后发生反应的离子方程式______.
(5)铝与氢氧化钠溶液反应的离子方程式为______.
SiO2和盐酸不反应,Fe2O3和氢氧化钠不反应而氧化铝能反应,该工艺流程原理为:铝土矿加入氢氧化钠,滤液C中含有偏铝酸根离子、硅酸根离子,A沉淀为氧化铁,B溶液中加过量盐酸,除去硅酸根离子,将偏铝酸根离子转化为铝离子,进入滤液C,沉淀D为硅酸,试剂乙为氨水,将铝离子转化为氢氧化铝沉淀,加热分解得氧化铝,
(1)工业上利用电解熔融的Al2O3 生成Al与氧气,以此冶炼金属Al,反应方程式为2Al2O3(熔融)
4Al+3O2↑, 电解 . 冰晶石
故答案为:电解熔融的Al2O3,2Al2O3(熔融)
4Al+3O2↑; 电解 . 冰晶石
(2)二氧化硅与氢氧化钠反应生成硅酸钠与水,反应离子方程式为:SiO2+2OH-═SiO32-+H2O,
氧化铝与氢氧化钠溶液反应生成偏铝酸钠与水,反应离子方程式为:Al2O3+2OH-═2AlO2-+H2O,
故答案为:SiO2+2OH-═SiO32-+H2O,Al2O3+2OH-═2AlO2-+H2O;
(3)由工艺流程可知,B溶液中加过量盐酸,除去硅酸根离子,将偏铝酸根离子转化为铝离子,进入滤液;
故答案为:除去硅酸根离子,将偏铝酸根离子转化为铝离子;
(4)氨水与铝离子反应生成氢氧化铝沉淀,反应离子方程式为:Al3++3NH3?H2O═Al(OH)3↓+3NH4+,
故答案为:Al3++3NH3?H2O═Al(OH)3↓+3NH4+;
(5)铝与氢氧化钠溶液反应生成偏铝酸钠与氢气,反应离子方程式为:2Al+2OH-+2H2O═2AlO2-+3H2↑,
故答案为:2Al+2OH-+2H2O═2AlO2-+3H2↑.
