小姚同学完成制取二氧化碳的实验后,对回收的盐酸和氯化钙混合溶液(不考虑其他杂质)进行了以下实验:取40g该溶液于烧杯中,滴入40g溶质质量分数为13.8%的K2CO3溶液.滴入K2CO3溶液质量与生成沉淀质量的关系如图所示.求:
(1)所取40g溶液中HCl和CaCl2的质量.
(2)当加入K2CO3的质量为30g时,所得溶液中溶质的质量分数
(3)实验结束后过滤,若将滤液蒸干,得到固体的质量.
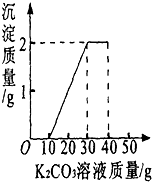
(1)从图象中的数据可以看出,10克之前没有出现沉淀,所以和盐酸反应的碳酸钾溶液是10克,从加入10g碳酸钾溶液开始出现沉淀,到30g后沉淀不变,说明和氯化钙反应的碳酸钾溶液是20克,生成沉淀是2克,
10g碳酸钾溶液中含有碳酸钾的质量为10g×13.8%=1.38g
设和碳酸钾反应的盐酸是X,生成氯化钾为y,生成二氧化碳的质量为z
K2CO3+2HCl═2KCl+H2O+CO2↑
138 73 14944
1.38gx y z
=138 1.38g
=73 x
=149 y 44 z
解得:x=0.73g,y=1.49g,z=0.44g
与氯化钙反应的碳酸钾的质量为:20g×13.8%=2.76g
设和碳酸钾反应的氯化钙为a,生成氯化钾为b,生成的碳酸钙质量为c
K2CO3+CaCl2═2KCl+CaCO3↓
138 111 149100
2.76g a b c
=138 2.76g
=111 a
=149 b 100 c
解得:a=2.22g;b=2.98g;c=2g
(2)当加入K2CO3的质量为30g时,所得溶液中溶质的质量分数为:
×100%=6.6%1.49g+2.98g 30g+40g-2g-0.44g
(3)反应后烧杯中的物质包括两个反应中生成的氯化钾,以及反应剩余的碳酸钾的质量,故:1.49g+2.98g+(40g-30g)×13.8%=5.85g.
答:(1)所取40g溶液中HCl的质量为0.73g;CaCl2的质量为1.48g.
(2)当加入K2CO3的质量为30g时,所得溶液中溶质的质量分数为6.6%.
(3)实验结束后过滤,若将滤液蒸干,得到固体的质量为5.85g.
