问题
问答题
某校兴趣小组的同学欲测定实验室中一瓶久置的过氧化氢溶液中溶质的质量分数.实验测得相关数据如图所示:
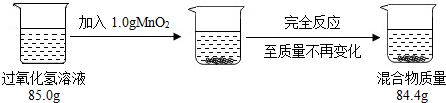
①反应结束后剩余的混合物中二氧化锰的质量为______g;生成氧气的质量为______g、物质的量为______mol.
②计算该过氧化氢溶液中溶质质量分数______(通过化学方程式列式计算).
答案
①因为催化剂在化学反应前后质量不变,故混合物中二氧化锰的质量为1.0g;根据质量守恒定律,反应生成氧气的质量=85g+1.0g-84.4g=1.6g;
物质的量是
=0.05mol;1.6g 32g/mol
②设68.0 g过氧化氢溶液中含有过氧化氢的质量为x.
2H2O2
2H2O+O2↑MnO2 .
68 32
x 1.6g
=68 x 32 1.6g
x=3.4g
过氧化氢溶液的溶质的质量分数=
×100%=4%;3.4g 85g
故答案为:①1.0;1.6;0.05;②4%;
