问题
问答题
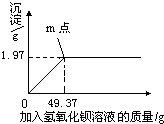
某校化学研究性学习小组在帮老师清理实验室时,发现一瓶氢氧化钠固体敞口露置在空气中,且表面出现白色粉末,他们断定这瓶氢氧化钠已经变质.学习小组的同学为测定其变质程度,设计了如下实验方案:①称取10.00g该样品②将称取的样品全部溶于水配成50.00g溶液③向②的溶液中滴加氢氧化钡[Ba(OH)2]溶液,并测得产生的碳酸钡沉淀与加入氢氧化钡溶液的质量关系如下图所示.试计算(计算结果精确到0.01%):
(1)所取样品中氢氧化钠的质量分数;
(2)m点溶液中溶质的质量分数.
答案
(1)由图象可知反应恰好完成时生成的沉淀质量是1.97g;
设:碳酸钠质量是x,生成氢氧化钠的质量是y
Na2CO3+Ba(OH)2═BaCO3↓+2NaOH
10619780
x1.97g y
=106 x
=197 1.97g 80 y
x=1.06g y=8g
则所取样品中氢氧化钠的质量分数为
×100%=89.4%;10.00g-1.06g 10.00g
(2)m点即为反应恰好完成点,则溶液中溶质的质量分数为:
×100%=10%;10.00g-1.06g+0.8g 50g+49.37-1.97g
答:(1)所取样品中氢氧化钠的质量分数为89.4%;(2)m点溶液中溶质的质量分数为10%.
