问题
问答题
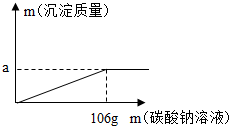
向138克CaCl2溶液中逐渐加入溶质质量分数为10%Na2CO3溶液至过量,经测得生成沉淀的质量与所加Na2CO3溶液的质量关系如图.
(1)计算a点的值?
(2)当两种溶液恰好完全反应时,所得溶液中溶质的质量分数?
答案
(1)反应中消耗的碳酸钠的质量=106g×10%=10.6g
设生成碳酸钙的质量为x,生成氯化钠的质量为y
Na2CO3+CaCl2═CaCO3↓+2NaCl
106 100 117
10.6gx y
=106 10.6g
=100 x 117 y
解得:x=10g,y=11.7g
所以a的值为10;
(2)反应后生成的溶液的溶质的质量分数为:
×100%=5%11.7g 138g+106g-10g
答:(1)a点的值为10;
(2)当两种溶液恰好完全反应时,所得溶液中溶质的质量分数为5%.
