问题
问答题
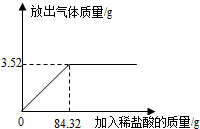
某学习小组取25g石灰石样品放人烧杯中,加人稀盐酸至不再产生气泡为止(石灰石中的杂质不溶于水,不含钙元素,也不与稀盐酸反应).加入稀盐酸的质量与放出气体质量的关系如图.
(1 )样品中的碳酸钙完全反应时消耗稀盐酸的质量为______g.
(2)加人稀盐酸至样品中的碳酸钙恰好完全反应(气体全部逸出),此时烧杯中溶液(含不溶性杂质)的总质量为______g.
(3)该石灰石样品中钙元素的质量是多少克?(规范写出计算过程)
答案
:(1)图象的转折点是二者恰好反应的点,观察图象可知此时用去稀盐酸的质量为84.32g;
故答案为:84.32g;
据图象可知:该样品最多与盐酸反应生成二氧化碳3.52g;
设碳酸钙的质量为x
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 44
x3.52g
=100 44 x 3.52g
解得:x=8g
(2)烧杯中溶液的总质量为:8g+84.32g-3.52g=88.8g
故答案为:88.8g;
(3)该石灰石样品中钙元素的质量为:8g×
×100%=3.2g40 40+12+16×3
答:该石灰石样品中钙元素的质量为3.2g.
