问题
问答题
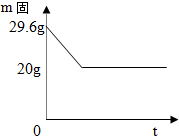
某实验小组,混合27.6g氯酸钾和2g二氧化锰,加热支取一定量氧气后撤去酒精灯,测得剩余固体质量如图所示.计算:
(1)制得氧气的质量为______g.
(2)氯酸钾分解的质量分数______(写出计算过程,结果精确到0.1%).
答案
(1)由质量守恒定律可知生成氧气的质量是29.6g-20g=9.6g;
(2)设分解的氯酸钾的质量为x
2KClO3
2KCl+3O2↑MnO2 . △
24596
x9.6g
=245 x 96 9.6g
x=24.5g
分解的氯酸钾的质量分数为:
×100%=88.8%24.5g 27.6g
答:氯酸钾分解的质量分数为88.8%.
故答案为:(1)9.6;(2)为88.8%.
