工业上电解饱和食盐能制取多种化工原料,其中部分原料可用于制备多晶硅.
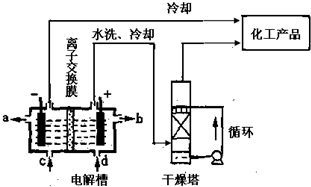
(1)图是离子交换膜法电解饱和食盐水示意图,电解槽阳极产生的气体是______;NaOH溶液的出口为______(填字母);精制饱和食盐水的进口为______(填字母);干燥塔中应使用的液体是______.
(2)多晶硅主要采用SiHCl3还原工艺生产,其副产物SiCl4的综合利用收到广泛关注.
①SiCl4可制气相白炭黑(与光导纤维主要原料相同),方法为高温下SiCl4与H2和O2反应,产物有两种,化学方程式为______.
②SiCl4可转化为SiHCl3而循环使用.一定条件下,在20L恒容密闭容器中的反应:3SiCl4(g)+2H2(g)+Si(g)

4SiHCl3(g)达平衡后,H2与SiHCl3物质的量浓度分别为0.140mol/L和0.020mol/L,若H2全部来源于离子交换膜法的电解产物,理论上需消耗纯NaCl的质量为______kg.
(3)采用无膜电解槽电解饱和食盐水,可制取氯酸钠,同时生成氢气,现制得氯酸钠213.0kg,则生成氢气______M3(标准状况).
(1)电解饱和食盐时阳极阴离子Cl-、OH-放电,Cl-的放电能力强于OH-,
阳极:2Cl--2e-═Cl2↑,
阴极:2H++2e-═H2↑;
总反应为:2NaCl+2H2O
Cl2↑+H2↑+2NaOH, 电解 .
阴极:氢离子放电,产生氢气.致使氢氧根离子浓度增大,钠离子和氢氧根离子的增大都发生在阴极室,所以a出口导出的液体是氢氧化钠溶液;
阳极:氯离子放电,产生氯气,致使钠离子浓度升高,通过阳离子交换膜到达阴极室.所以d入口应加入精制饱和食盐水;
要干燥Cl2需要用酸性干燥剂浓硫酸或P2O5等,中性干燥剂无水CaCl2.
(2)①SiCl4与H2和O2反应,产物有两种,光导纤维的主要成分是SiO2,H、Cl元素必在另一产物中,H、Cl元素结合成HCl,然后配平即可.
发生的化学方程式为:SiCl4+2H2+O2
SiO2+4HCl; 高温 .
②由3SiCl4(g)+2H2(g)+Si(s)

4SiHCl3(g)
起始量(mol) n 0
变化量(mol) 2x x 4x
平衡量(mol) n-2x 4x
4x=0.020mol/L×20L=0.4mol,x=0.1mol,
n-2x=0.140mol/L×20L=2.8mol,n=3.0mol,
由2NaCl+2H2O
Cl2↑+H2↑+2NaOH, 电解 .
2mol 1mol
=2×58.5g 1mol
; m(NaCl)=351g=0.351kg.m(NaCl) 3mol
(3)由NaCl转化为NaClO3,失去电子数为6,H2O转化为H2,得到的电子数为2,
设产生的H2体积为Vm3,
由得失电子守恒得:6×
=2×213×103g 116.5gmol-1
; Vm3×103L•m-3 22.4L•mol-1
V=134.4m3.
故答案为:(1)①氯气;a;d;浓硫酸;
(2)①SiCl4+2H2+O2
SiO2+4HCl;②0.351; 高温 .
(3)134.4.
