问题
计算题
将盛有50g稀盐酸的烧杯放在天平上,然后把过量的碳酸钠加入到盛有稀盐酸的烧杯中,以测定稀盐酸中HCl的质量分数。已知反应前烧杯内稀盐酸和碳酸钠的总质量为60.0g, 从反应开始至以后的6分钟内,每1分钟读1次数并记录。结果如下:
| 时间/min | 0 | 1 | 2 | 3 | 4 | 5 | 6 |
| 质量/g | 60.0 | 58.0 | 57.0 | 56.8 | 56.7 | 57.2 | 56.7 |
(1)表中有一个测定结果误差较大,这点所在的时间是第_______min;
(2)在给出的坐标纸上,画出表示反应过程的质量与时间的曲线图;
(3)试计算50g稀盐酸中HCl的质量分数(写出计算过程)。
答案
(1)5;(2)见图;(3)11%(或10.95%)。

:(1)过量碳酸钠与稀盐酸反应时,烧杯内物质的总质量应先逐渐减小,最后保持不变.由于第5分钟时烧杯内物质总质量增大,说明测定结果误差较大.
(2)见图
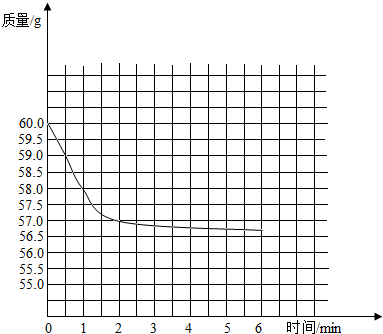 ;
;
(3)设稀盐酸中溶质的质量分数为x.
Na2CO3+2HCl=2NaCl+H2O+CO2↑
73 44
50g×x 60.0g-56.7g
| 73 |
| 44 |
| 50g×x |
| 60.0g-56.7g |
答:(3)稀盐酸中溶质的质量分数为10.95%.
