铝是一种应用广泛的金属,工业上用Al2O3和冰晶石(Na3AlF6)混合熔融电解制得.
①铝土矿的主要成分是Al2O3和SiO2等.从铝土矿中提炼Al2O3的流程如图1所示:
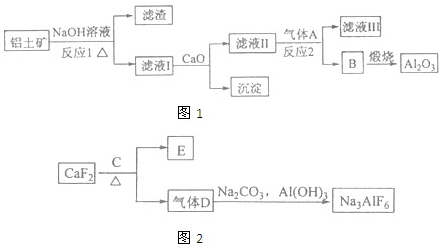
②以萤石(CaF2)和纯碱为原料制备冰晶石的流程如图2所示:
回答下列问题:
(1)写出反应1的化学方程式______;
(2)滤液Ⅰ中加入CaO生成的沉淀是______,反应2的离子方程式为______;
(3)E可作为建筑材料,化合物C是______,写出由D制备冰晶石的化学方程式______;
(4)电解制铝的化学方程式是______,以石墨为电极,阳极产生的混合气体的成分是______.
(1)二氧化硅与氢氧化钠反应生成硅酸钠与水,反应方程式为:2NaOH+SiO2=Na2SiO3+H2O,氧化铝与氢氧化钠反应生成偏铝酸钠与水,反应方程式为:2NaOH+Al2O3=2NaAlO2+H2O,
故答案为:2NaOH+SiO2=Na2SiO3+H2O、2NaOH+Al2O3=2NaAlO2+H2O;
(2)滤液Ⅰ中含有硅酸钠、偏铝酸钠,加入CaO,生成氢氧化钙,氢氧化钙与硅酸钠反应生成硅酸钙沉淀;
由工艺流程可知,B为氢氧化铝,故气体A为二氧化碳,滤液Ⅱ主要是偏铝酸钠,偏铝酸钠溶液通入二氧化碳,生成氢氧化铝与碳酸钠,反应方程式为:2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32-,
故答案为:CaSiO3;2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32-;
(3)由工艺流程可知,气体C含有F元素,应是HF,故C为浓硫酸;根据元素守恒,可知HF与碳酸钠、氢氧化铝反应生成冰晶石,同时生成二氧化碳、水,反应方程式为:12HF+3Na2CO3+2Al(OH)3=2Na3AlF6+3CO2+9H2O,
故答案为:浓H2SO4;12HF+3Na2CO3+2Al(OH)3=2Na3AlF6+3CO2+9H2O;
(4)电解熔融的氧化铝生成铝与氧气,反应方程式为:2Al2O3(熔融)
4Al+3O2↑,阳极生成氧气,部分氧气可以石墨反应生成二氧化碳、CO,故阳极气体有O2、CO2(或CO) 通电 . 冰晶石
故答案为:2Al2O3(熔融)
4Al+3O2↑;O2、CO2(或CO). 通电 . 冰晶石
