(6分)硅酸钠(Na2SiO3)是我国优先发展的精细化工产品,工业制备的反应为:
2NaOH+ SiO2 ="=" Na2SiO3 + H2O 。现以125t石英砂(SiO2质量分数为96%)为原料,与
足量的NaOH溶液反应。试计算:
(1)125t石英砂中SiO2的质量。
(2)理论上得到硅酸钠的质量。
(6分)解:(1)石英砂中的SiO2的质量=125t×96%=120t(2分)
(2)设生成硅酸钠的质量为x
2NaOH + SiO2 == Na2SiO3 + H2O
60 122
120t x
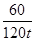 =
=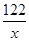
X="244t" ……………………………………………………4分
答:略。
(1)根据石英砂中SiO2质量分数为96%,由石英砂的质量计算其中SiO2的质量;(2)根据反应的化学方程式,利用石英砂中SiO2的质量计算反应可生成硅酸钠的质量。
【解答】解:(1)石英砂中的SiO2的质量=125t×96%=120t
(2)设生成硅酸钠的质量为x
2NaOH+SiO2═Na2SiO3+H2O
60 122
120t x
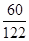 =
= x=244t
x=244t
答:(1)125t石英砂中SiO2的质量为120t;
(2)理论上得到硅酸钠的质量为244t。
【点评】根据化学方程式进行计算时,所使用的物质的质量应为纯净物的质量,不可把混合物的质量直接代入进行计算。
