问题
计算题
⑴H2O2中氢、氧原子个数比为 ;
⑵在实验室里用68克溶质质量分数为5%的H2O2溶液与少量MnO2混合制取氧气,计算生成氧气的质量。
答案
⑴l:1(或2:2)
⑵解:设可生成氧气的质量为x,
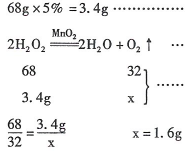
答:生成氧气的质量为1.6g。
分析:(1)物质中各元素的原子个数比一般为化学式中各元素原子的角码比.
(2)利用过氧化氢制氧气的化学方程式,根据过氧化氢的质量求出氧气的质量.
解答:解:(1)一个过氧化氢分子是由两个氢原子和两个氧原子构成的.故答案为1:1(或2:2).
(2)设生成氧气的质量为x
2H2O2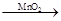 2H2O+O2↑
2H2O+O2↑
68 32
68g×5%=3.4g x
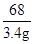 =
=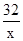 ,x=1.6g
,x=1.6g
答:可生成氧气1.6g.
点评:物质中各元素的原子数目之比和物质中各元素的质量比要区分清楚,原子数目比一般为化学式中各原子的角码之比,而元素的质量比需要通过计算才能得到.
