凤凤的初中玉玉同学认为Ca (OH)2与CO2能反应,而NaOH与CO2不能反应,因为实验室检验CO2只用澄清石灰水而不用NaOH溶液.凤凤同学认为玉玉同学的说法不完全正确.凤凤同学怎么通过实验证明自己的观点呢?请你与凤凤同学一起在实验室完成以下实验.
(1)[提出假设]NaOH溶液能与CO2反应.
(2)[设计方案]
①用试剂______和______制取CO2气体;
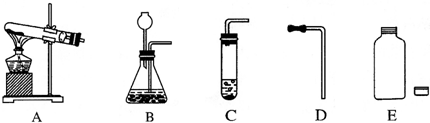
②请你从如图所示装置中选出正确的制取CO2的发生装置______(填字母),不选择其他发生装置的理由是______.
用图中的D和E(橡皮导管与塑料瓶)与发生装置组装来收集CO2气体的作法是______.
③[验证假设]
| 实验步骤 | 实验现象 | 结论 |
| 第一步:向集满CO2的塑料瓶中注入少量NaOH溶液,立即旋好盖子,振荡. | ______; | NaOH溶液吸收了塑料瓶中的CO2气体. |
| 第二步:取上一步中所得溶液,加入盐酸. | ______. | 化学方程式:______ |
(3)[总结反思]
实验室里NaOH溶液易变质,易变质的原因是______(用化学方程式表示).所以NaOH溶液应密封保存.
设计方案①实验室制取二氧化碳的药品是:石灰石(或大理石)和稀盐酸;
②根据反应物的状态和反应条件是固液常温型,故在和C中选,但B装置错误:长颈漏斗未伸入液面下,导气管太长,故不选;
故答案为:C;制取二氧化碳是固液常温型,故不选A,而B中的长颈漏斗未伸入液面下,导气管太长,故不选B;
因为二氧化碳的密度比空气大,易溶于水,所以采用向上排空气法收集;这儿用塑料瓶代替集气瓶,具体做法为:将导气管伸入到塑料瓶的底部.
验证假设:第一步 因氢氧化钠与二氧化碳反应,是塑料瓶内的气压变小,所以大气压把塑料瓶压扁;故答案为:塑料瓶变扁
第二步 氢氧化钠与二氧化碳反应生成碳酸钠,加盐酸会产生二氧化碳,故答案为:产生气泡 Na2CO3+2HCl═2NaCl+H2O+CO2↑
总结反思 因为氢氧化钠溶液易吸收二氧化碳而变质,应密封保存.方程式为:2NaOH+CO2=Na2CO3+H2O
故答案为:设计方案 ①石灰石(或大理石)和稀盐酸; ②C 制取二氧化碳是固液常温型,故不选A,而B中的长颈漏斗未伸入液面下,导气管太长,故不选B;将导气管伸入到塑料瓶的底部.
验证假设 塑料瓶变扁 产生气泡 Na2CO3+2HCl═2NaCl+H2O+CO2↑
总结反思 2NaOH+CO2=Na2CO3+H2O
