问题
计算题
把4g硫粉放在给定质量的氧气中燃烧,有关实验数据如下表所示,请回答问题:
| 第一次 | 第二次 | 第三次 | |
| 氧气的质量(g) | 3 | 4 | 6 |
| 二氧化硫的质量(g) | 6 |
(2)请你通过计算求出第二次.第三次实验生成的SO2的质量,填入表中。
答案
(1)1:1:2 (2)8
本题考查的是根据化学反应方程式的计算,根据质量守恒定律,在化学反应中,参加反应前各物质的质量总和等于反应后生成各物质的质量总和。
(1)由图表数据可知,第一次参加反应的S的质量=生成的SO2的质量-O2的质量,所以第一次参加反应的S的质量=6g-3g=3g;所以第一次实验中,参加反应的S、O2、生成的SO2三种物质的质量比为:3g:3g:6g=1:1:2;
(2)设第二次实验中,参加反应的S的质量为x,
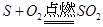
32 32
x 4g
32/32 ="x/4g"
x=4g
则第二次实验生成SO2的质量为:4g+4g=8g;因为只有4g硫粉,由第二次实验的计算可知,4g硫粉与给定质量的氧气完全反应,生成8gSO2,故第三次实验生成SO2的质量应为8g。
