李明在学习了碱溶液的化学性质后,做了如下实验:
在两个气密性良好且盛满二氧化碳的相同的矿泉水瓶中,分别注入10mL的饱和石灰水和浓NaOH溶液,充分振荡,发生了下图所示现象.
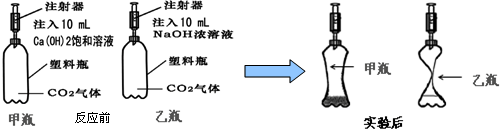
(1)甲瓶中发生反应的化学方程式为:______;
(2)甲、乙瓶中实验现象的不同之处是______;
(3)实验中若发现有矿泉水瓶无变瘪现象,则可能的原因是______;
(4)李明受上述实验启发,设计了一套检验、除去一氧化碳中混有的二氧化碳,并收集较为纯净一氧化碳的装置(下图).根据李明所设计的实验目的,要求:
广口瓶②中所加入的试剂应是:
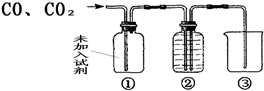
______;
广口瓶①中所加入的试剂的量应为:______(选填:
瓶、半瓶、满瓶、任意量).1 3
(1)氢氧化钙与二氧化碳反应生成碳酸钙沉淀和水,化学方程式为:Ca(OH)2+CO2=CaCO3↓+H2O
(2)氢氧化钙与二氧化碳反应生成碳酸钙沉淀,因此石灰水变浑浊,氢氧化钠与二氧化碳反应生成碳酸钠溶于水,不变浑浊,氢氧化钙微溶于水,氢氧化钠易溶于水,等体积的两溶液中含氢氧化钠多,吸收二氧化碳多,因此乙瓶变瘪的程度比甲瓶大.
(3)装置气密性良好的情况下,若药品变质,则就会出现无变瘪现象.
(4)除去一氧化碳中混有的二氧化碳,而用氢氧化钠溶液吸收二氧化碳,瓶中液体半瓶即可,通过浓氢氧化钠溶液除去二氧化碳的同时混入了水蒸气,因此2瓶内应盛浓硫酸来干燥一氧化碳.
故答案为:(1)Ca(OH)2+CO2=CaCO3↓+H2O
(2)甲中溶液变浑浊,乙中溶液未变浑浊,乙瓶变瘪的程度比甲瓶大.
(3)药品变质.
(4)浓硫酸;半瓶.
