问题
计算题
将30g碳酸钠溶液与48.2g氯化钡溶液混合,碳酸钠和氯化钡两种物质恰好完全反应。过滤,所得滤液质量为58.5g,试计算:
(1)反应后生成的沉淀质量为 克.
(2)所得滤液中溶质的质量分数为多少?(用百分数表示,写出计算过程。)
答案
(1) 19.7 (2)20%
根据质量守恒,生成的沉淀的质量为反应前后溶液质量之差,为30g+48.2g-58.5g=19.7g。已知沉淀BaCO3的质量,根据化学方程式求出反应后的NaCl的质量,又知道所得滤液质量为58.5g,则求出滤液中溶质的质量分数。
(2) 解:设溶液中溶质NaCl的质量为x
Na2CO3+BaCl2="2NaCl" + BaCO3↓
117 197
x 19.7g
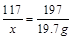
x=11.7g
滤液中溶质的质量分数为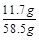 ×100%=20%
×100%=20%
