问题
计算题
乙醇俗称酒精,可用作医用消毒,也常作燃料。其完全燃烧的化学方程式可表示为:C2H6O+3O2 2 CO2+ 3 H2O 。
2 CO2+ 3 H2O 。
23g乙醇完全燃烧需消耗多少克氧气?
乙醇不完全燃烧会产生一氧化碳,某实验测得反应前后各物质的质量如下表:
| 物质 | 乙醇 | 氧气 | 二氧化碳 | 水 | 一氧化碳 |
| 反应前质量(g) | 4.6 | 8.8 | 0 | 0 | 0 |
| 反应后质量(g) | 0 | 0 | 6.6 | 5.4 | a |
①表中a的值为____ __。
②该实验发生反应的化学方程式为:4C2H6O+11O2 _____ CO2+ _____ H2O + _____ CO 。
_____ CO2+ _____ H2O + _____ CO 。
答案
(1) 48g
(2) ①1.4 ② 6 12 2
根据化学方程式可计算出23gC2H6O完全燃烧需氧气48g,根据质量守恒定律,可计算出反应后一氧化碳的质量为1.4g,参加反应的乙醇分子和反应生成的二氧化碳分子的数目比为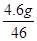 ∶
∶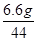 =2∶3,所以②的反应中二氧化碳的化学计量数为6,根据碳元素守恒可知,一氧化碳的化学计量数为2,根据氢元素守恒可知水的化学计量数为12。
=2∶3,所以②的反应中二氧化碳的化学计量数为6,根据碳元素守恒可知,一氧化碳的化学计量数为2,根据氢元素守恒可知水的化学计量数为12。
(1)解:设氧气质量X
C2H6O + 3O2 2CO2 + 3H2O
2CO2 + 3H2O
46 96
23g X
46:96=23g:X X=48g
答:氧气质量48g

 总量和热量
总量和热量