问题
计算题
(6分)某含有杂质的CaCO3固体(杂质不溶于水,也不与酸反应),老师安排同学做测定该固体混合物中CaCO3质量分数的实验.利用电子天平测定的有关实验数据如下表:
| 称量项目 | 质量/g |
| 杂质和 CaCO3的混合物 | 10.00 |
| 锥形瓶+稀盐酸(适量) | 141.20 |
| 锥形瓶+稀盐酸+杂质和CaCO3的混合物 (反应开始后15秒) | 149.20 |
| 锥形瓶+稀盐酸+杂质和CaCO3的混合物 (反应开始后35秒) | 149.00 |
| 锥形瓶+稀盐酸+杂质和CaCO3的混合物 (反应开始后55秒) | 149.00 |
(2)试通过分析计算固体混合物中CaCO3的质量分数?
答案
(1)2.2g(2)50%
题目分析:根据化学反应前后质量守恒,可以求出CO2质量为:10g+141.2g-149.0g=2.2g 固体中碳酸钙和稀盐酸反应放出了二氧化碳,所以可以由二氧化碳的质量,根据 化学方程式求出碳酸钙的质量,再进一步求出碳酸钙的质量分数。
设生成2.2gCO2需要CaCO3质量为x
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 44
X 2.2g
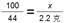
x=5g
CaCO3质量分数= ×100%=50%.
×100%=50%.
答:生成二氧化碳2.2克,样品中碳酸钙的质量分数是50%.。
