下面是工厂苛化法生产烧碱的示意图。

(1)在实验室,操作Ⅰ的名称是 ;经操作Ⅰ得到废渣的主要成份是 (写化学式)。
(2)物质X中各元素的质量比表示为 。
(3)某工厂化验员向含有1.6 g氢氧化钠的溶液中,逐滴加入20.0 g盐酸至氢氧化钠和盐酸恰好完全反应。求盐酸中溶质的质量分数为多少?(写出过程)
(4)若用1.6 g上述得到的固体烧碱产品(含杂质)代替1.6 g氢氧化钠,逐滴加入上述相同浓度盐酸至反应物恰好完全反应,则消耗盐酸的质量 20 g(填“大于”、“等于”或“小于”)。
(1)过滤 CaCO3 (2)氢元素质量∶氧元素质量=1∶8 (3)7.3% (4)大于
题目分析:(1)在实验室,操作Ⅰ的名称是过滤,其依据是固液分离;经操作Ⅰ得到废渣的主要成份是CaCO3 ;(2)由题中的叙述可知物质X为水,故(2)物质X中各元素的质量比表示为氢元素质量∶氧元素质量=1∶8
(3)设盐酸中溶质的质量为x
NaOH + HCl="NaCl" + H2O (1分)
40 36.5
1.6 g x
40∶36.5==1.6 g ∶x
x=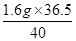 =1.46 g (1分)
=1.46 g (1分)
盐酸中溶质的质量分数为 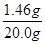 ×100% =7.3%
×100% =7.3%
(4)若用1.6 g上述得到的固体烧碱产品(含杂质)代替1.6 g氢氧化钠,逐滴加入上述相同浓度盐酸至反应物恰好完全反应,则消耗盐酸的质量大于20g
