黄铜矿(CuFeS2)是制取铜及其化合物的主要原料之一,还可制备硫及铁的化合物。
(1) 冶炼铜的反应为
若CuFeS2中Fe的化合价为+2,反应中被还原的元素是__________(填元素符号)。
(2) 上述冶炼过程产生大量SO2。下列处理方案中合理的是________(填代号)
a.高空排放 b.用于制备硫酸 c.用纯碱溶液吸收制Na2SO3 d.用浓硫酸吸收
(3)过二硫酸钾(K2S2O8)具有强氧化性.可将I-氧化为I2:S2O32-十2I-=2SO42-+I2:通过改变反应途径,
Fe3+、Fe2+均可催化上述反应。试用离子方程式表示Fe3+对上述反应催化的过程______________________________(不必配平)
(4) 利用黄铜矿冶炼铜产生的炉渣(含Fe2O3、FeO、SiO2、Al2O3)可制备Fe2O3。
方法为①用稀盐酸浸取炉渣,过滤。②滤液先氧化,在加入过量NaOH溶液,过滤,将沉淀洗涤、干燥、煅烧得Fe2O3
据以上信息回答下列问题:
a. 除去Al3+的离子方程式是__________________。
b.选用提供的试剂,设计实验验证炉渣中含有FeO。
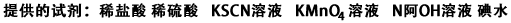
所选试剂为_______________。证明炉渣中含有FeO的实验现象为__________
(1)Cu、O
(2)bc
(3)2Fe3++2I-=2Fe2++I2、S2O82-+Fe2+=2SO42-+2Fe3+
(4)a.Al3++4OH-=AlO2-+2H2O[或Al3++4OH-=Al(OH)-;b.稀硫酸、KMnO4溶液稀硫酸浸取炉渣所得溶液使
KMnO4溶液褪色
