(9分)有一铝粉和Fe3O4粉末组成的铝热剂,在隔绝空气的条件下加热使之充分反应。将反应后所得混合物研细,并分成均匀的两等份,在一份中加足量的氢氧化钠溶液,另一份中加入足量的盐酸,反应后,前者消耗m mol NaOH,放出气体0.336 L;后者消耗n mol HCl,放出气体V L,若将等质量的铝热剂直接与足量稀硫酸作用,可得3.36 L气体(上述气体体积均已换算成标准状况)。试求铝热剂中Al的质量分数。
28.0%
(1)铝热剂直接与H2SO4作用时产生气体的反应如下:
2Al + 3 H2SO4 = Al2(SO4)3 + 3 H2↑
54.0 g 67.2 L
m(Al) 3.36 L
列式可解得:m(Al)=2.70 g
铝热反应后的混合物遇NaOH能放出H2,表明铝热反应Al剩余,则:
2Al + 2NaOH + 6H2O = 2Na [Al(HO)4] + 3 H2↑
54.0 g 67.2 L
m(Al) 0.336 L
列式可求得:m余(Al)=0.540 g
铝热剂中Fe3O4的质量可求:
3 Fe3O4 + 8 Al 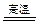 4 Al2O3 + 9 Fe
4 Al2O3 + 9 Fe
696 g 216 g
m(Fe3O4) 2.70g-0.540g
列式可求得:m(Fe3O4)=6.96 g
则:w(Al)=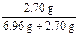 ×100%=28.0%
×100%=28.0%