问题
填空题
铜是重要的金属材料。
(1)工业上可用Cu2S和O2反应制取粗铜,该反应中氧化剂为 _______ 。电解粗铜制取精铜,电解时.阳极材料是 _______ ,电解液中必须含有的阳离子是 _______ 。
(2)在100 mL 18 mol/L浓硫酸中加入过量的铜片,加热使之充分反应,反应中被还原的H2SO4< __ mol。
(3)电子工业曾用30%的FeCl3溶液腐蚀敷有铜箔的绝缘板制印刷电路板,为了从使用过的废腐蚀液中回收铜,并重薪得到FeCl3溶液,设计如下实验流程。
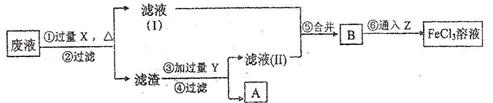
上述流程中,所加试剂的化学式为:X _______ ,Y _______ Z _______ ;第⑥步反应的离子方程式为 _______ 。
答案
(1)Cu2S 、O2;粗铜 ; Cu2+
(2)0.9
(3)X-Fe ;Y- HCl; Z- Cl2; 2Fe2++Cl2=2Fe3++2Cl-
(2)共含硫酸1.8mol。但该反应因硫酸不足量而停止,实际参与反应的硫酸小于1.8mol,而被还原的硫酸又只是参加反应硫酸的一半,故被还原的硫酸小于0.9mol。
