(11分)实验室需要0.1 mol/L NaOH溶液450 mL和0.5 mol/L硫酸溶液450 mL.根据这两种溶液的配制情况回答下列问题:
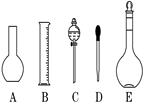
(1)如图所示的仪器中配制溶液肯定不需要的是 (填序号),
仪器C的名称是 ,
本实验所需玻璃仪器E规格为 mL。
(2)下列操作中,容量瓶所不具备的功能有 (填序号)。
A.配制一定体积准确浓度的标准溶液
B.长期贮存溶液
C.用来加热溶解固体溶质
D.量取一定体积的液体(3)在配制NaOH溶液实验中,其他操作均正确。若定容时仰视刻度线, 则所配制溶液浓度
0.1 mol/L(填“大于”“等于”或“小于”,下同)。若NaOH溶液未冷却即转移至容量瓶定容,则所配制溶液浓度 0.1 mol/L。
(4)根据计算得知,所需质量分数为98%、密度为1.84 g/cm3的浓硫酸的体积为 mL(计算结果保留一位小数)。如果实验室有10 mL、25mL、50 mL量筒,应选用 mL规格的量筒最好。
(1) AC(1分) 分液漏斗(1分)
(2) 500ml (2分) BCD (2分)
(3) < >(2分)
(4)13.6 (2分 ) 25(1分)
考查溶液的配制
(1)在配制过程中,不需要A:平底烧瓶、C:分液漏斗
根据容量瓶的规格可知,选用略大于450ml的,即500ml
(2)容量瓶唯一的作用就是配制溶液,没有其它作用,故BCD符合题意
(3)定容时仰视刻度线,会导致加水偏多,浓度偏小。
若NaOH溶液未冷却即转移至容量瓶,由于热膨胀,定容时加少量会偏少,最终溶液浓度偏高
(4)0.5×0.5=V×1.84×98%/98,求得V=13.6ml;很明显,应选用容积略大于13.6ml的25ml量筒
