问题
填空题
(2分)微粒模型观察与比较。如下图所示,在钠与氯气的反应中,每个钠原子失去1个电子,成为1个钠离子;每个氯原子得到1个电子,成为1个氯离子;钠离子与氯离子结合形成氯化钠。因为1个电子的质量大约为1个质子或中子质量的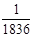 ,故原子的质量几乎都集中在原子核上。
,故原子的质量几乎都集中在原子核上。
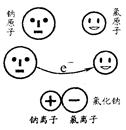
若用r、m分别表示微粒的半径和质量,以“<”或“>”或“≈”填空。
(1) m(Na) m(Na+); (2) r(Cl) r(Cl-);
(3) r(Na) r(C1); (4) r(Na+) r(Cl-)。
答案
(2分,每空0.5分)
(1)≈(2)<(3)>(4)<
题目分析:同周期的元素一般满足从左往右半径依次减小,因为半径越小,对电子的吸附能力就越强,外围的电子数就越多;离子核外电子层数越多离子半径越大。
(1)1个电子的质量大约为1个质子或中子质量的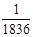 ,故原子的质量几乎都集中在原子核上,所以m(Na)≈m(Na+);
,故原子的质量几乎都集中在原子核上,所以m(Na)≈m(Na+);
(2)因为Cl离子比Cl原子多了1个电子,所以Cl离子的半径大于Cl原子的半径;r(Cl)<r(Cl-);
(3)根据同周期的元素一般满足从左往右半径依次减小,可知:r(Na)>r(C1);
(4)比较离子的半径大小:第一看离子核外电子层数,层数越多离子半径越大;第二,如果电子层数相同,看核电荷数,核电核数越大对外界电子的吸引力越大,离子半径反而越小。Na+只有两层电子层,Cl-有三层,因此:r(Na+)<r(Cl-)。
点评:同周期的元素一般满足从左往右半径依次减小,本题难度较大。
